Содержание
- Что такое рак желудка?
- Анатомия желудка и его функции
- Факторы риска развития рака желудка
- Симптомы
- Диагностика
- Определение стадии рака желудка
- Лечение
- Динамическое наблюдение
- Профилактика
Что такое рак желудка?
Раком желудка называют злокачественную опухоль, развивающуюся из клеток слизистой оболочки желудка, а именно, из железистых клеток слизистой оболочки желудка. Такой рак называют железистым или - аденокарциномой.
Согласно современным представлениям о возникновении злокачественных опухолей причина их появления – это мутационные изменения генетического аппарата клетки.
В норме рост клеток ограничен – они делятся некоторое количество раз, после чего умирают, а на смену им приходят новые, молодые клетки. Но у раковых клеток, из-за повреждения структуры генома, отсутствуют механизмы, сдерживающие их деление. В результате клетки начинают делиться бесконтрольно, формируя массив опухоли. В дальнейшем, увеличивающаяся в объеме опухоль прорастает всю стенку желудка, затем прорастает в ближайшие органы и ткани, нарушая их нормальную работу.
В подавляющем большинстве случаев одно злокачественное новообразование развивается из одной опухолевой клетки.
Существуют также опухоли желудка, которые происходят из соединительной ткани и отличаются от рака желудка (например, гастроинтестинальные стромальные опухоли (ГИСО)).
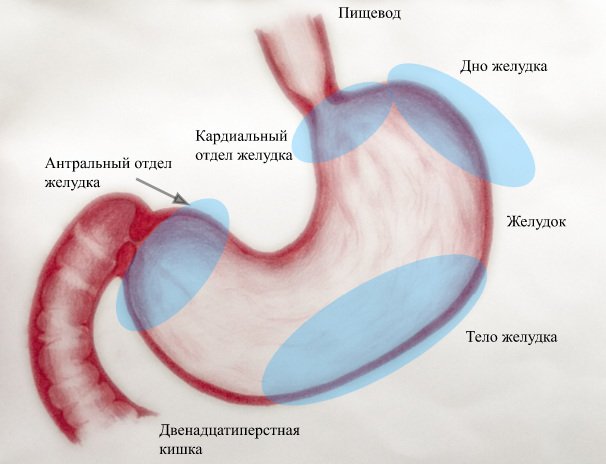
Рис. 1. Строение желудка
Код заболевания рак желудка по МКБ-10: С 16 (злокачественная опухоль желудка).
Анатомия желудка и его функции
Желудок – это полый мышечный орган, расположенный в пищеварительном тракте между пищеводом и двенадцатиперстной кишкой. Топографически желудок располагается в верхней части живота. Стенка желудка состоит из 4 слоев: внутренний слой – слизистая оболочка (1), располагающаяся на подслизистой основе (2), следующий слой - мышечный (мышечная оболочка(3)), и наружный (внешний слой) – серозный (4).
Начальный отдел желудка - кардиальная часть желудка, куда, через кардиальное отверстие, поступает пищевой комок из пищевода. Далее желудок расширяется, образуя дно, или свод, который книзу переходит в тело желудка. Нижний выпуклый край желудка формирует большую кривизну, верхний вогнутый — малую кривизну. Узкая правая часть желудка образует привратник (пилорус), который далее переходит в двенадцатиперстную кишку и отделен от нее пилорическим сфинктером.
Желудок играет важную роль в процессе пищеварения. Здесь выделяется соляная кислота и многие ферменты, необходимые для переваривания пищи. Благодаря мышечным сокращениям стенок желудка еда измельчается и тщательно перемешивается с желудочным соком, после чего, порционно поступает дальше в тонкую кишку – для последующего процесса пищеварения.
Факторы риска развития рака желудка
- Воспалительные изменения стенки желудка - на фоне хронического гастрита, язвенной болезни желудка, дуодено-гастрального рефлюкса может развиваться опухолевая трансформация клеток и появиться рак. При гастрите и язвенной болезни желудка, как правило, повышенная концентрация соляной кислоты вызывает воспалительные изменения в нормальной структуре слизистой оболочки желудка, повреждает ее. При дуодено-гастральном рефлюксе происходит заброс кишечного содержимого из двенадцатиперстной кишки (дуоденум) в желудок, чего в норме не происходит. Содержимое двенадцатиперстной кишки значительно отличается по своим физико-химическим характеристикам от содержимого желудка, поэтому, попадая в желудок – вызывает повреждение слизистой оболочки желудка.
- Хеликобактерная инфекция. Данная инфекция возникает, когда бактерия Helicobacter pylori поселяется и размножается (колонизирует) на слизистой оболочке желудка. Данная бактерия способна стимулировать выработку желудком соляной кислоты и фермента пепсина. Соляная кислота в высокой концентрации вызывает воспалительные изменения в нормальной структуре слизистой оболочки желудка, повреждает ее, что проявляется сначала гастритом, а в некоторых случаях приводит к развитию язвы желудка. Если не лечить данные заболевания, и не устранить причину их вызвавшую (бактерию), то это может привести к мутационным изменениям генетического аппарата клеток слизистой оболочки желудка. Риск возникновения рака желудка у инфицированных больных H. pylori. в 3,8 раза выше по сравнению с неинфицированными.
- Кишечная метаплазия желудка - состояние, при котором клетки (эпителий) нормальный слизистой оболочки желудка замещаются клетками, которые в норме составляют слизистую оболочку двенадцатиперстной кишки. Процесс этот происходит на границе желудка и двенадцатиперстной кишки, как правило, этому способствует дуодено-гастральный рефлюкс.
- Наличие полипа или полипов желудка. Полип желудка представляет собой образование, растущее из стенки желудка в его просвет. Как правило, клинические проявления отсутствуют.
- Диета с высоким содержанием соленой, острой, копченой пищи, а также низким содержанием фруктов и овощей, чрезмерное употребление алкоголя, употребление в пищу продуктов с повышенным содержанием консервантов и нитратов.
- Курение.
- Наличие генетической предрасположенности (если раком желудка болел родственник первой степени родства - мать, отец, сестра или брат). Установлено, что во многих семьях, где кто-то уже страдал заболеванием, оно появляется не только в следующем поколении, но и проявляется через несколько поколений.
Развитие рака желудка чаще происходит у мужчин и пожилых людей старше 60 лет.
Наличие у Вас того или иного фактора риска вовсе не означает, что рак желудка непременно разовьется. Но, людям, попадающим в группы риска, следует внимательней относиться к своему здоровью - скорректировать образ жизни и пройти необходимые исследования.
Симптомы
Симптомы рака желудка можно разделить на две группы: ранние и поздние.
- Ранние симптомы рака желудка:
- Повышенная утомляемость, общая слабость
- Тошнота
- Дискомфорт в верхней части живота в проекции желудка
- Вздутие живота после еды
- Снижение аппетита
- Изжога
- Поздние симптомы рака желудка:
- Примесь крови к калу (черный стул)
- Рвота
- Потеря веса
- Боли в верхней части живота (в желудке)
- Чувство переполнения желудка при приеме небольшого количества пищи
- Отрыжка
- Желтуха (пожелтение кожи и глаз)
- Увеличение живота в объеме за счет накопления жидкости в брюшной полости (проявление асцита)
Также, указать на злокачественный процесс в желудке может выявление отдаленных метастазов, характерных для рака желудка:
- Метастаз Вирхова – метастаз в надключичные лимфатические узлы.
- Метастаз Шницлера – метастаз располагается в пространстве между маткой и прямой кишкой (у женщин) или мочевым путем и прямой кишкой (у мужчин). Метастаз можно выявить при пальцевом ректальном исследовании.
- Метастаз Крукенберга – метастазы рака желудка в яичники.
- Метастаз сестры Джозеф – метастаз опухоли в пупок.
Во всех случаях необходимо подтверждение наличия метастазов путем их биопсии и гистологической верификации (подтверждение наличия в образовании измененных опухолевых клеток при микроскопическом исследовании).
При появлении первых признаков рака желудка, сомнениях и подозрениях на заболевание следует как можно скорее обратиться в клинику для проведения диагностики. В нашем Хирургическом отделении N2 Университетской клинической больницы N4 есть все самое современное оборудование и высококвалифицированные специалисты, которые смогут поставить точный диагноз.
Диагностика
- Общий осмотр. Диагностика заболевания начинается с осмотра пациента, включающую в себя поверхностную и глубокую пальпацию живота, пальпацию в проекции лимфатических узлов.
- Сбор анамнеза болезни. Сбор врачом сведений о том как протекало заболевание, о том какие симптомы появлялись и/или сменяли друг друга и на каком этапе совокупность симптомов и изменения состояния пациента привело к обращению за помощью в медицинское учреждение.
- Изучение анамнеза жизни. Сбор врачом сведений о ранее перенесенных заболеваниях, операциях, о наличии хронических болезней и их течении, принимаемых в связи с этими болезнями лекарственных препаратов. Уточняется семейный анамнез – в первую очередь уточняют болел ли кто из родственников первой степени родства раком желудка. На этом этапе врач, в том числе, определяет наличие или отсутствие в течение жизни у пациента факторов риска, которые могли привести к развитию рака желудка.
- Инструментальные методы диагностики:
- Эзофагогастродуоденоскопия (ЭГДС) – данная процедура выполняется с помощью тонкой и гибкой трубки с лампочкой и видеокамерой на ее конце - гастроскопа. При помощи гастроскопа можно с разрешением высокого качества осмотреть пищевод, желудок и двенадцатиперстную кишку. При выявлении измененного участка слизистой оболочки желудка выполняется его биопсия. При помощи биопсийных щипцов, во время гастроскопии, из подозрительного участка слизистой оболочки желудка берут кусочек ткани для последующего гистологического исследования.
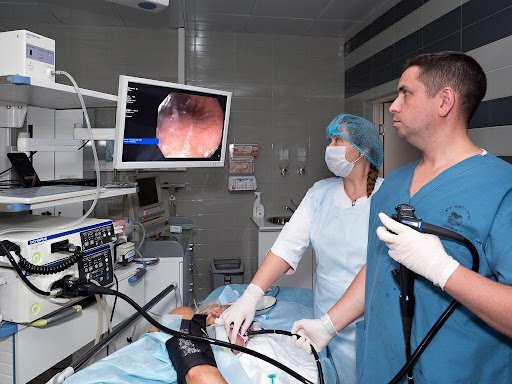
Фото 1. Процедура эзофагогастроскопии
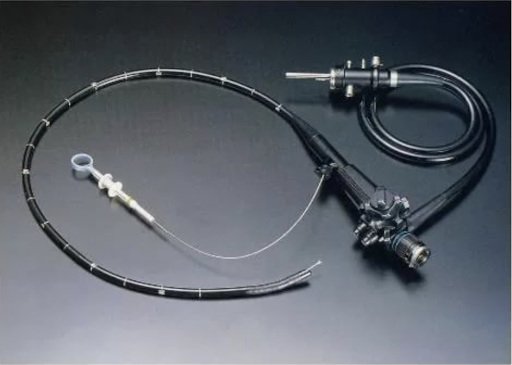
Фото 2. Гастроскоп
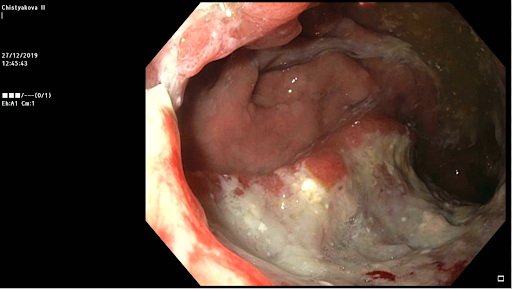
Фото 3. Рак-язва желудка2 диагностированный при гастроскопии
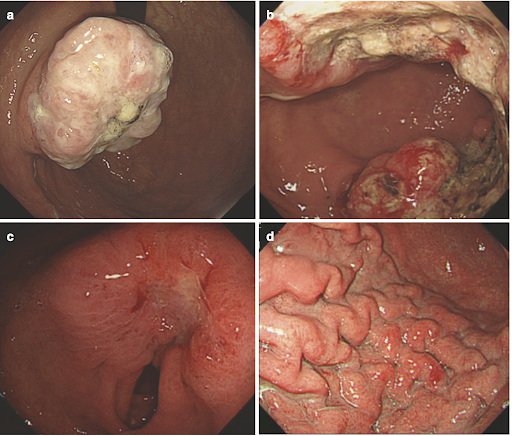
Фото 4. Изменения слизистой оболочки желудка выявляемые при гастроскопии1
- УЗИ (ультразвуковое исследование). При этом методе исследования используется специальный прибор, в котором с помощью специального генератора воспроизводятся высокочастотные звуковые волны (ультразвук), которые распространяются вглубь организма. Одновременно, с помощью специального датчика, регистрируется ультразвуковой сигнал от внутренних органов и тканей. Эхо-сигналы, после компьютерной обработки, формируют ультразвуковую картину на экране монитора, которую видит и оценивает специалист – врач ультразвуковой диагностики. Метод позволяет оценить распространенность рака желудка, выявляет значительно увеличенные лимфатические узлы, расположенные рядом с желудком.
- Эндосонография (эндоскопическое ультразвуковое исследование) – это процедура, схожая с гастроскопией. Однако, на конце эндоскопа установлен ультразвуковой датчик и генератор ультразвука. Прибор позволяет более точно определить насколько глубоко опухоль поражает стенку желудка (есть ли полное прорастание), прорастает ли опухоль в соседние органы (поджелудочная железа, пищевод и т.д.), а также определить наличие лимфоузлов пораженных метастазами - по сравнению с обычным ультразвуковым исследованием.
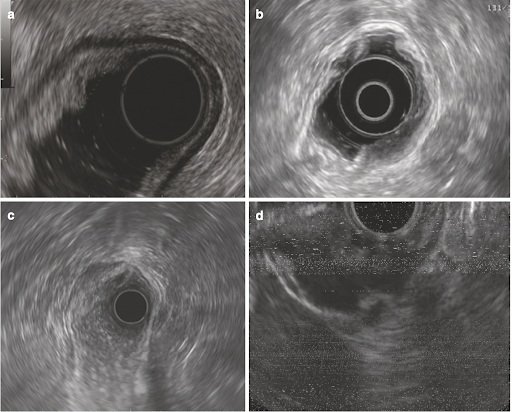
Фото 5. Изображение получаемое при эндосонографии1
- Рентгенологическое исследование желудка с барием. В ходе данного исследования пациент выпивает жидкость содержащую специальное рентгенконтрастное вещество – сульфат бария, после чего пациенту делают рентгеновский снимок. Принятый внутрь барий равномерно заполняет желудок и на рентгеновских снимках неизмененного желудка определяется ровный рельеф слизистой оболочки желудка. При наличии язвы желудка или рака желудка на снимке будет виден измененный рельеф слизистой оболочки.
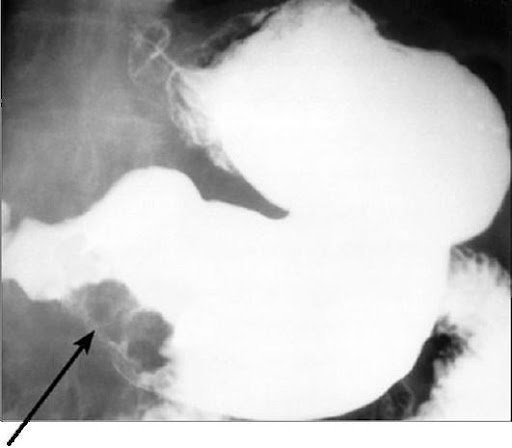
Фото 6. Рентгеноскопия. Стрелкой отмечен «дефект заполнения», изменения контура желудка.
Мультиспиральная компьютерная томография (МСКТ) грудной клетки и брюшной полости (с внутривенным контрастированием).
Сканирование этих двух областей организма человека, выполняемые, как правило, последовательно в течение одного исследования, помогают определить распространенность рака желудка, наличие или отсутствие метастазов в такие органы как печень и легкие, а также установить вовлеченность в процесс отдаленных от желудка групп лимфатических узлов. Общая точность метода при установлении стадии заболевания составляет более 50% и является стандартом уточняющей диагностики при раке желудка в большинстве развитых стран.
У пациентов с раком желудка компьютерная томография обычно проводится для предоперационной оценки и определения стадии опухоли. В частности, технические разработки в области КТ, такие как многодетекторная спиральная КТ (МДКТ), трехмерная (3D) рефракция и КТ-ангиография, обеспечивают детальное стадирование опухоли, хирургическое картирование и предоперационную оценку анатомии сосудов.
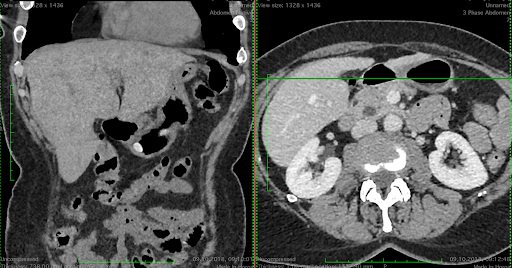
Фото 7. Изображения, полученные при мультиспиральной компьютерной томографии с внутривенным контрастированием. Изображение получено в двух проекциях. Стрелками отмечен желудок.
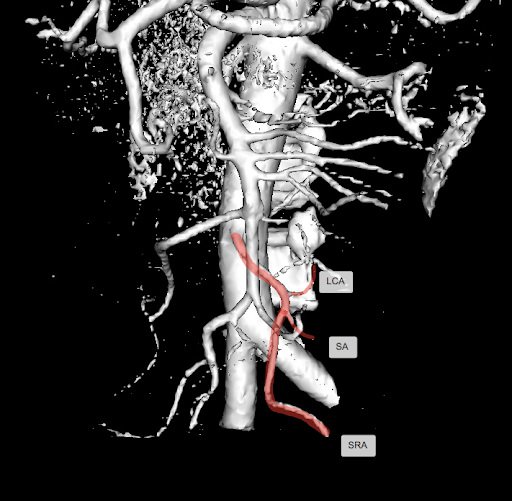
Фото 8. 3-D реконструкция сосудов, получена в результате компьютерной обработки изображений, полученных при мультиспиральной компьютерной томографии с внутривенным контрастированием.
- ПЭТ (позитронно-эмиссионная томография) – это процедура, с помощью которой определяют наличие злокачественной опухоли и ее метастазов в организме человека, выполняется по показаниям. Метод основан на том, что клетки раковой опухоли за счет своей повышенной активности (ускоренного метаболизма) накапливают введенную глюкозу быстрее и больше чем нормальные ткани. В ходе данного исследования определенное количество раствора радиоактивной глюкозы вводят внутривенно. После сканирования всего организма и обработки цифровых данных компьютером получают изображение тела человека, на котором пораженные злокачественными клетками органы и ткани светятся ярким светом. ПЭТ и КТ могут быть выполнены одновременно - это называется ПЭТ-КТ.
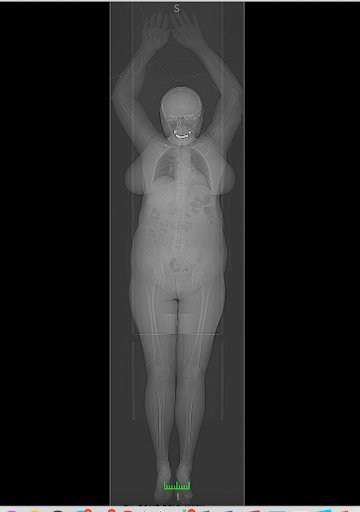
Фото 9. Изображение при ПЭТ-КТ.
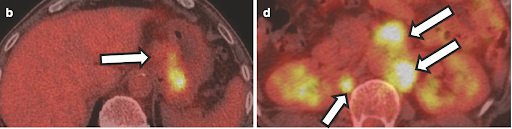
Фото 10. Изображение при ПЭТ-КТ. Стрелками отмечена ткань с активным метаболизмом (опухоль).
- Колоноскопия – выполняется для исключения синхронных опухолей толстой кишки у пациентов старше 50 лет при планировании радикального хирургического лечения рака желудка.
- Остеосцинтиграфия – исследование выполняется при подозрении на метастатическое поражение костей. Является методом радионуклидной диагностики, основанный на введении в организм пациента тропного к костной ткани радиофармацевтического препарата и последующей регистрации его распределения и накопления в скелете с помощью гамма-излучения изотопа, входящего в состав препарата.
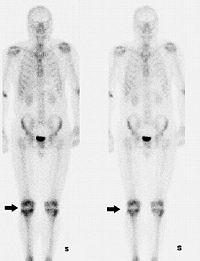
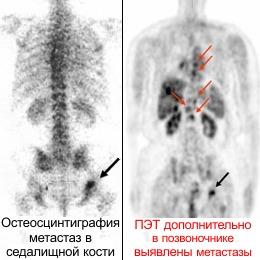
Фото 11. Изображение при остеосцинтиграфии. 1 - Стрелочками отмечены зоны активного накопления радионуклидов костной тканью в суставных концах костей образующих коленные суставы (норма). 2 – метастаз в седалищной кости.
- Биопсия метастатических очагов или очагов подозрительных как метастатические под контролем УЗ_аппарата и компьютерной томографии.
- Диагностическая лапароскопия - показана при раке желудка IB-III стадий. Выполняется для уточнения глубины поражения стенки желудка, распространения ее на соседние органы, выявления мелких очагов опухоли на оболочке, покрывающей внутренние органы, мелких метастазов в печени, селезенке, яичниках. Также во время этой процедуры собирают свободную жидкость из брюшной полости для определения опухолевых клеток в ней.
- Гистологическое (патоморфологическое) исследование позволяет установить диагноз рака желудка. Исследуют биопсийный материал, взятый при эндоскопической биопсии (в ходе эзофагогастродуоденоскопии, эндо-узи), либо после биопсии очагов подозрительных в отношении их метастатического поражения (например биопсии печени в ходе лапароскопии). При помощи световой микроскопии, после предварительной окраски микропрепаратов, определяют гистологический тип опухоли.
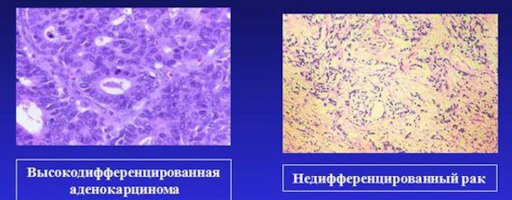
Фото 12. Различные варианты рака желудка (световая микроскопия).
Существует определенная градация аденокарциномы желудка по степени дифференцировки опухолевых клеток:
Gx – степень дифференцировки клеток не может быть оценена
G1 – высокодифференцированный рак
G2 – умереннодифференцированный рак
G3 – низкодифференцированный рак
G4 – недифференцированный рак
В процессе дифференцировки менее специализированная клетка становится более специализированной. Дифференцировка меняет функцию клетки, её размер, форму и метаболическую активность. Уровень (степень) дифференцировки опухолевых клеток связывают с понятием злокачественности опухоли. В свою очередь, степень злокачественности раковой опухоли является прогностическим фактором.
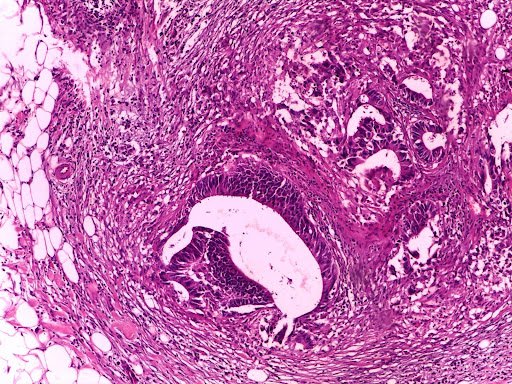
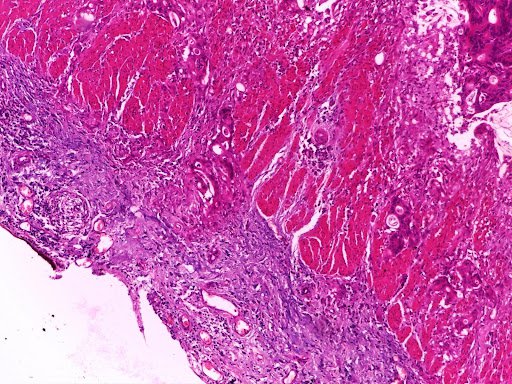
Фото 13,14. Умереннодифференцированная аденокарцинома кишечного типа (световая микроскопия).
Лабораторные методы диагностики:
- Определяется уровень онкомаркеров СА72-4, СА19-9, РЭА. Наличие в организме раковой опухоли желудка, особенно на поздних стадиях, когда злокачественные клетки попадают в лимфатическую систему или кровь, сопровождается появлением в организме специфических белков-антигенов, которые могут быть обнаружены при выполнении специального лабораторного анализа - определения уровня онкомаркера. Уровень онкомаркеров позволяет отследить ответ на лечение или заподозрить возврат заболевания при неуклонном росте его значений в процессе наблюдения после проведенного лечения.
- Общий анализ крови
- Общий анализ мочи
- Биохимический анализ крови
При подготовке пациентов к хирургическому лечению с целью оценки текущего функционального статуса организма могут назначаться дополнительные исследования – ЭКГ (электрокардиография), ЭхоКГ (УЗИ сердца), суточное холтеровское мониторирование ЭКГ и артериального давления (АД), функциональные нагрузочные тесты (тредмил-тест), МСКТ сердца, исследование функции внешнего дыхания (ФВД), УЗИ сосудов (вен и/или артерий) нижних конечностей.
Обязательными лабораторными исследованиями перед хирургическим этапом лечения являются – исследование свертывающей системы крови, определение наличия в крови маркеров инфекций - сифилиса, гепатитов В и С, вируса иммунодефицита человека (ВИЧ), определение группы крови по системе АВ0 и резус-фактора, фенотипа.
По показаниям проводятся консультации специалистов – терапевта, кардиолога, уролога, гастроэнтеролога, невролога, нефролога, пульмонолога.
Определение стадии рака желудка
Для установления стадии рака желудка необходимо провести ряд необходимых диагностических исследований. По результатам проведенных исследований врач определяет насколько обширно распространение раковой опухоли.
Чтобы говорить на одном понятном для всех специалистов языке в большинстве стран мира, в повседневной практике используют систему буквенных (T, N и М, а также a, b, и c) и цифровых (от 0 до 4) символов для обозначения стадии рака любой локализации, в том числе и рака желудка. В настоящее время используется TNM-классификация седьмого пересмотра.
Все варианты развития рака желудка попадают в одну из пяти возможных стадий (от стадии 0 до стадии IV). Стадия процесса определяется на основании всех полученных ранее данных: глубина прорастания стенки желудка опухолью, вовлеченности в процесс соседних тканей и органов, лимфатических узлов, а также распространением на отдаленные органы (печень, легкие и др.).
| Tx |
Первичная опухоль не может быть оценена |
| T0 |
Данных о наличии первичной опухоли нет |
| Tis |
Опухоль растет в пределах слизистой оболочки без инвазии в собственную пластинку / тяжелая дисплазия эпителия - карцинома in situ |
| T1 |
Опухоль прорастает собственную пластинку или мышечную пластинку слизистой оболочки, подслизистый слой. |
| T1a |
Опухоль прорастает собственную пластинку или мышечную пластинку слизистой оболочки |
| T1b |
Опухоль прорастает подслизистый слой, но не выходит за ее пределы |
| T2 |
Опухоль прорастает мышечный слой стенки желудка |
| T3 |
Опухоль прорастает мышечный слой полностью, но не выходит за пределы серозной (наружной) оболочки желудка, нет инвазии (прорастания) в соседние органы. Но, к этой группе относятся опухоли с прорастанием в желудочно-ободочную и желудочно-печеночную связку, большой и малый сальник - без поражения висцеральной брюшины. |
| T4 |
Опухоль прорастает наружную (серозную) оболочку (висцеральную брюшину) и/или соседние органы, забрюшинное пространство. |
| T4a |
Опухоль прорастает наружную (серозную) оболочку (висцеральную брюшину) |
| T4b |
Опухоль прорастает в соседние органы, такие как печень, селезенка, поперечная ободочная кишка, поджелудочная железа, диафрагма, надпочечник, почка, тонкая кишка, прорастание в забрюшинное пространство, переднюю брюшную стенку. |
| Nx |
Регионарные лимфатические узлы не могут быть оценены |
| N0 |
Нет метастазов в регионарных лимфатических узлах |
| N1 |
Поражение 1-2 регионарных лимфатических узлов |
| N2 |
Поражение 3-6 регионарных лимфатических узлов |
| N3 |
Поражение более 7 регионарных лимфатических узлов |
| N3a |
Поражение 7-15 регионарных лимфатических узлов |
| N3b |
Поражение более 15 регионарных лимфатических узлов |
| Mх |
Наличие отдаленных метастазов не может быть оценено |
| M0 |
Отдаленные метастатзы отсутствуют |
| M1 |
Наличие отдаленных метастазов, либо наличие опухолевых клеток в смывах /биоптатах с брюшины |
После того, как врач ознакомится с результатами ваших исследований, он получит возможность сгруппировать все три символа с их индексами в единое целое. Совокупность этих обозначений позволит ему определить клиническую стадию рака желудка в конкретном случае.
Стадии рака желудка в соответствии с группировкой индексов:
| Стадия 0 |
Tis |
N0 |
M0 |
| Стадия IA |
T1 |
N0 |
M0 |
| Стадия IB |
T2 |
N0 |
M0 |
|
T1 |
N1 |
M0 |
| Стадия IIA |
T3 |
N0 |
M0 |
|
T2 |
N1 |
M0 |
|
T1 |
N2 |
M0 |
| Стадия IIB |
T4a |
N0 |
M0 |
|
T3 |
N1 |
M0 |
|
T2 |
N2 |
M0 |
|
T1 |
N3 |
M0 |
| Стадия IIIA |
T4a |
N1 |
M0 |
|
T3 |
N2 |
M0 |
|
T2 |
N3 |
M0 |
| Стадия IIIB |
T4b |
N0, N1 |
M0 |
|
T4a |
N2 |
M0 |
|
T3 |
N3 |
M0 |
| Стадия IIIC |
T4b |
N2, N3 |
M0 |
|
T4a |
N3 |
M0 |
| Стадия IV |
Любое T |
Любое N |
M1 |
До получения результатов патоморфологического исследования врач устанавливает стадию рака желудка исключительно по данным инструментальных методов исследования, что с высокой степенью вероятности, позволяет правильно разработать программу лечения конкретного пациента. На этом этапе определяется КЛИНИЧЕСКАЯ стадия заболевания. Она является лишь предварительной. В медицинской документации клиническая стадия обозначается префиксом «с».
Пример клинического диагноза: Рак желудка cT3N2M0, IIIA стадия.
Окончательно стадия заболевания устанавливается на основании данных исследования удаленного операционного материала (фрагмента желудка или всего желудка с опухолью и лимфатическими узлами, удаленными фрагментами других органов с метастазами) врачом-патоморфологом в отделении патоморфологии, поэтому она носит название ПАТОМОРФОЛОГИЧЕСКОЙ. В медицинской документации патоморфологическая стадия обозначается префиксом «p».
Пример диагноза: Рак желудка pT3N2M1 (метастаз в S4 печени), IV стадия.
В случае, если интраоперационно не выявлено отдаленных метастазов, и они отсутствуют по данным инструментальных методов исследования, то в диагнозе, после проведения патоморфологического исследования удаленного препарата, возле литеры М сохраняется префикс «с».
Пример диагноза: Рак желудка pT3N2 cM0, IIIA стадия.
Лечение
Выбор тактики лечения определенного онкологического пациента в Клинике колопроктологии и малоинвазивной хирургии осуществляется на мультидисциплинарном онкологическом консилиуме с участием онколога, хирурга, эндоскописта, химиотерапевта, анестезиолога, терапевта, с учетом результатов дооперационного обследования, с определением клинической стадии заболевания и функционального состояния пациента. Тактика лечения определяется стадией и состоянием пациента.
Основным методом радикального лечения рака желудка является хирургический, дополняемый в большинстве случаев системной противоопухолевой терапией (химиотерапией).
Ранний рак желудка
К раннему раку желудка относятся следующие клинические стадии заболевания - cTisN0M0 (стадия 0) и cT1аN0M0 (первая стадия рака желудка - IA). На данных стадиях опухолевые клетки определяются только в пределах слизистой оболочки (поверхностный слой) желудка. Особенностью данной группы является благоприятный прогноз после хирургического лечения: 5-летняя выживаемость составляет более 90%. Это означает что 90% всех пациентов с диагностированным ранним раком после радикального хирургического лечения живут 5 лет и более.
В данных случаях показано хирургическое лечение в объеме эндоскопической резекции (удаления) слизистой оболочки желудка (EMR) либо эндоскопическая слизисто-подслизистая диссекция (ESD) - если позволяет размер и расположение опухоли.
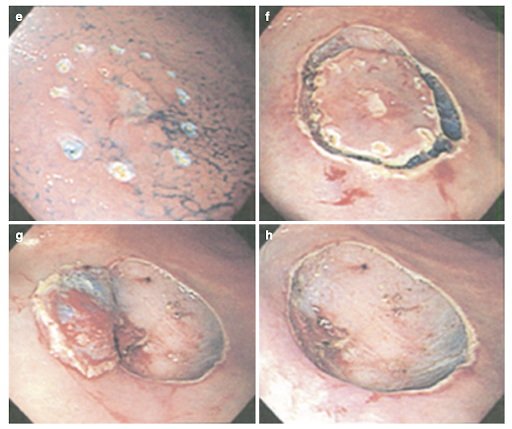
Фото 15 (e-h). Этапы эндоскопической резекции желудка1
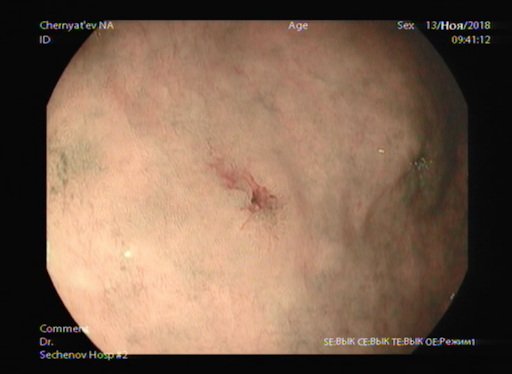
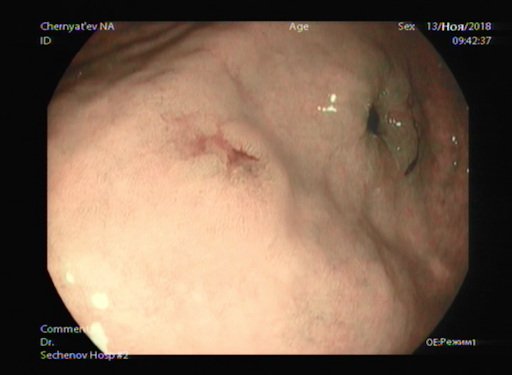
Фото 16,17. Ранний рак желудка2
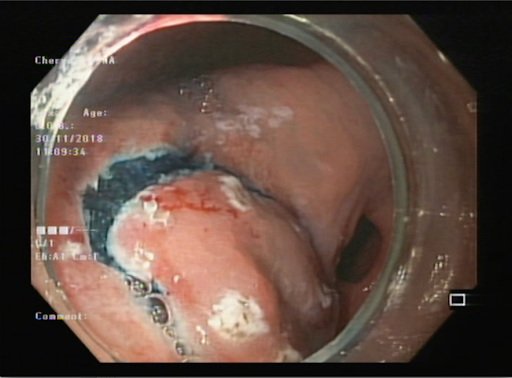
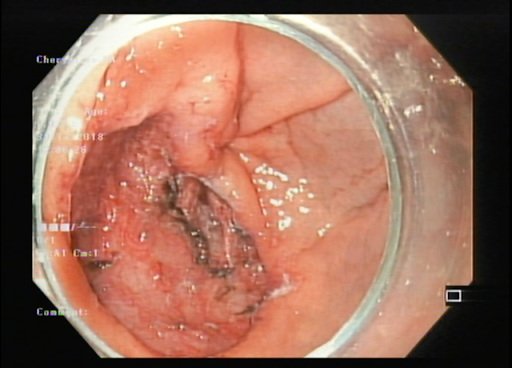
Фото 18,19. Ранний рак желудка, этапы слизисто-подслизистой диссекции -ESD (эндоскопическое удаление)2
При значительных размерах опухоли (более 2см) используется неэндоскопические варианты хирургического лечения, а именно удаление части желудка – резекция желудка. Кроме этого, показанием для резекции желудка на этих стадиях может стать нерадикальное хирургическое лечение с помощью видеоэндоскопических методов – в случае обнаружения при патоморфологическом (гистологическом) исследовании опухолевых клеток по краю резекции, признаков прорастания опухоли в сосуды, подслизистый слой желудка.
Резекция желудка может выполняться различными способами:
- Открытая хирургия – осуществляется через широкий разрез передней брюшной стенки.
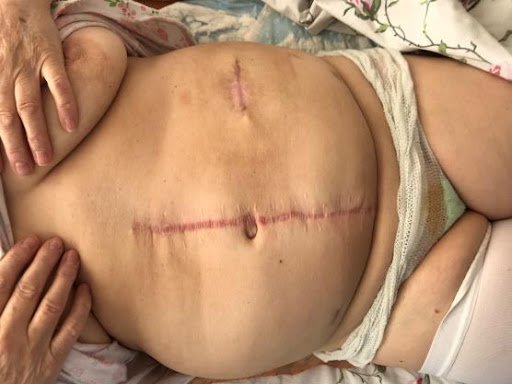
Фото 20. Послеоперационный рубец передней брюшной стенки (открытая хирургия)
- Лапароскопическая хирургия – оперативное пособие осуществляется с помощью специальных лапароскопических хирургических инструментов через маленькие проколы в передней брюшной стенке.
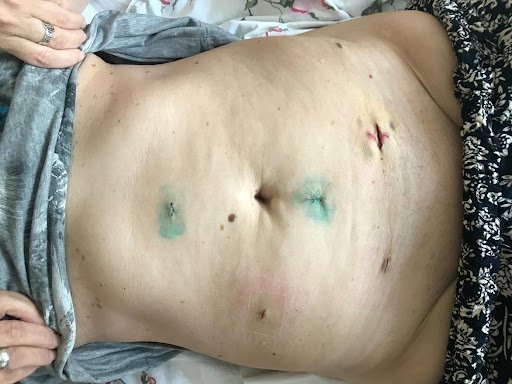
Фото 21. Послеоперационные рубцы передней брюшной стенки (лапароскопическая хирургия)
- Роботическая хирургия - оперативное пособие осуществляется с помощью роботической системы DaVinci через маленькие проколы в передней брюшной стенке.
Рак желудка IB-IIIC стадий («поздний» рак желудка)
Основным методом лечения II стадии рака желудка является хирургический, при этом выполняют хирургическую резекцию (удаление) части желудка (проксимальная или дистальная резекция), реже – удаление всего органа. При высоком риске развития отдаленных метастазов используется комбинированный метод лечения: хирургическое лечение с последующим проведением курсов химиотерапии.
Для лечения III стадия рака желудка чаще применяется комбинированный метод лечения – хирургическое лечение, дополненное периоперационной или адъювантной (послеоперационной) химиотерапией.
Выбор вида операции зависит от целого ряда факторов, к числу которых относятся факторы, связанные с характеристиками опухоли и со стадией заболевания, с общим состоянием организма заболевшего человека, и с квалификацией врачей, принимающих непосредственное участие в лечении.
Общие принципы
Каждый хирург, выполняющий хирургическое лечение рака желудка, производит удаление опухоли и минимизирует негативные последствия самого хирургического вмешательства. Благоприятный исход может быть достигнут при соблюдении следующих правил:
- Полное удаление опухоли с частью пораженного органа (резекция) или удаление всего желудка целиком (гастрэктомия), при этом, не допускают разрушения опухоли или контакта опухоли с внутренними органами во время операции
- Выполнение лимфодиссекции – удаление лимфатических узлов, которые могут содержать раковые клетки ввиду возможного распространения опухолевых клеток по лимфатическим сосудам. Лимфатические узлы располагаются в жировой клетчатке, прилежащей к желудку, а также в клетчатке, которая расположена по ходу сосудов (артерий и вен желудка)
- Если это возможно, удаляются все метастатические очаги, расположенные в других органах (опухолевые метастазы), чем обеспечивается радикальное лечение, либо максимальное уменьшение опухолевой массы в организме (циторедукция), для создания благоприятных условий для последующего лечения. В некоторых случаях выполняется удаление целых органов вместе с метастатическим очагом (например, селезенки), чаще выполняется удаление органа с метастатическим очагом (например, резекция определенного сегмента печени с метастазом)
- Восстановление пассажа пищевого комка по кишечнику, то есть восстановление целостности (непрерывности) пищеварительного тракта
Виды операций при раке желудка IB-IIIC стадий
- Резекция желудка (проксимальная или дистальная) с лимфодиссекцией:
Удаление верхней или нижней пораженной части желудка вместе с близлежащими лимфатическими узлами и окружающей их жировой клетчаткой. Данная операция выполняется только по строгим медицинским показаниям, так как значительно ухудшает качество жизни пациента в послеоперационном периоде.
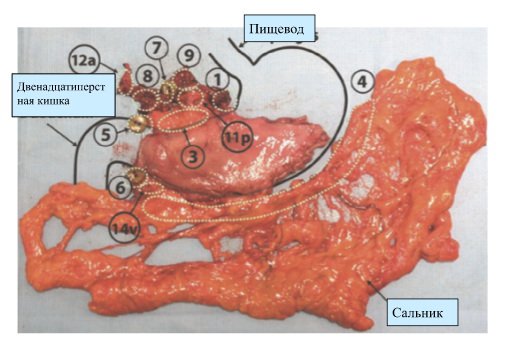
Фото 22. Рак желудка, вид удаленного препарата2
- Гастрэктомия с расширенной лимфодиссекцией:
При данном виде хирургического лечения выполняется полное удаление желудка вместе с опухолью, близлежащими лимфатическими узлами и окружающей жировой клетчаткой (лимфодиссекция). Операция может сопровождаться удалением (частичным или полным) прилежащих к желудку органов - в случае прорастания в них опухоли. После полного удаления желудка с раковой опухолью формируют анастомоз (соединение) между пищеводом и тонкой кишкой, восстанавливая таким образом целостность кишечного тракта для осуществления пищеварительной функции.
Резекция желудка может выполняться различными способами:
- Открытая хирургия – осуществляется через широкий разрез передней брюшной стенки.
- Лапароскопическая хирургия. При этом способе лечения хирург через отдельные маленькие проколы на передней брюшной стенке вводит в брюшную полость специальные инструменты, с помощью которых, под контролем видеокамеры, выполняет оперативное пособие. Во время операции хирургическая бригада получает увеличенное изображение на экранах мониторов в 2D или 3D режимах визуализации.
- Роботическая хирургия. При этом способе лечения операция также, как и при лапароскопии, выполняется через маленькие проколы на передней брюшной стенке, однако, в качестве инструмента хирург использует сложнейший роботизированный комплекс с 3D-визуализацией (объемное изображение).
- Хирургический метод лечения резектабельного рака желудка в настоящий момент продолжает оставаться основным. Только хирургическое лечение в 2018 году в России получили 71,9% больных. После радикального хирургического лечения, согласно данным американского сообщества популяционных раковых регистров SEER, 5-летняя выживаемость составляет при 1А стадии - 95%, 1B стадии - 85%, 2 стадии - 54%, 3А стадии - 37%, 3Б стадии - 11%.
Рак желудка, IV стадия
Вся группа пациентов IV стадией рака желудка очень неоднородна. Следует сразу заметить, что прогноз у пациентов данной группы неблагоприятный. Однако, в последние годы произошел большой скачок в развитии фармацевтической науки. Поэтому, комбинированное лечение помогает облегчить жизнь пациентов с IV стадией рака желудка и увеличить продолжительность их жизни.
Варианты лечения пациентов с раком желудка IV стадии:
- хирургическое лечение с удалением опухоли желудка и отдаленных метастазов с последующим курсом химиотерапии.
- Различные варианты паллиативной хирургии, направленной на улучшение качества жизни пациентов, у которых на мультидисциплинарном онкологическом консилиуме, или интраоперационно (во время попытки хирургического лечения) опухоль признается неоперабельной, либо паллиативная хирургия при возникновении жизнеугрожающих состояний – осложнений опухолевого процесса: перфорации желудка, кровотечения, развития опухолевого стеноза.
Например, при перекрытии опухолью пищеводно-желудочного отверстия, вследствие чего возникает невозможность проглатывания пищи, устанавливается специальное устройство – стент, который расширяет и сохраняет просвет пищевода и обеспечивает прохождение пищи. При перекрытии опухолью гастродуоденального отверстия (хода, через который осуществляется выход пищи из желудка) - хирургически формируется гастроэнтероанастамоз (специально сообщение (соустье) между желудком и тонкой кишкой, через которое в дальнейшем осуществляется прохождение пищи).
- Паллиативная химиотерапия.
- Переход первично неоперабельного местнораспространенного рака в операбельное состояние в результате реализации эффекта лекарственной противоопухолевой терапии.
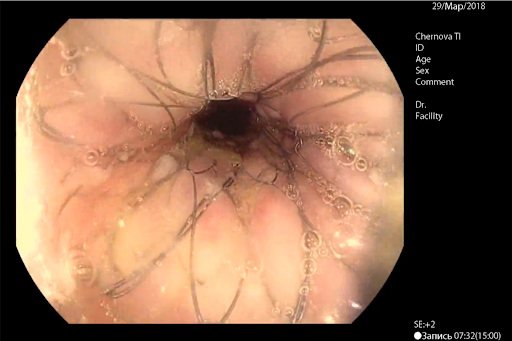
Фото 23. Неоперабельный рак желудка с сужением просвета и нарушением проходимости, вид после установки стента2
Химиотерапия (лекарственная противоопухолевая терапия)
Химиотерапия – это метод лечения с применением лекарственных препаратов, способных убивать опухолевые клетки или же останавливать их деление и рост.
Препараты вводятся внутривенно в условиях дневного стационара. Так как препараты действуют не только на опухолевые, но и на здоровые клетки организма, то проведение химиотерапевтического лечения оказывает токсическое воздействие на организм, что проявляется (или может проявиться) многочисленными токсическими эффектами. Как правило, одновременно вводятся несколько противоопухолевых препаратов, что позволяет снизить дозу каждого из них, а следовательно, и уменьшить выраженность побочных эффектов каждого отдельно взятого химиотерапевтического препарата.
Химиотерапевтическое лечение применяется (комбинируется) в сочетании с хирургическим лечением (до или после операции). Целесообразно применение химиотерапии при показателях сT3-4N0 и cT-любое N1-3. Чаще всего проводят 4 курса химиотерапии перед операцией и 4 курса – после оперативного лечения.
Преимущества предоперационной химиотерапии включают в себя:
- Уничтожение опухолевых клеток и/или снижение их злокачественного потенциала.
- Уменьшение размеров опухоли.
- Снижение риска местного возврата (рецидива) рака.
- Улучшение качества подготовки к операции за счет восстановления проходимости через зону опухоли (при наличии стеноза) - при больших новообразованиях.
Нежелательные последствия предоперационной химиотерапии:
- Общая токсичность, проявляющаяся в виде тошноты, рвоты, плохого самочувствия, изменениях в лабораторных показателях крови (снижение уровня лейкоцитов, тромбоцитов).
- Повышение риска тромбозов вен и тромбоэмболии легочной артерии.
- Повышение риска переломов костей.
- Повышение риска внезапной клинической смерти у пациентов старческого возраста или с тяжелыми сердечно-сосудистыми заболеваниями.
Паллиативная химиотерапия – показана для лечения первично неоперабельного местнораспространенного рака, либо метастатического рака желудка. Выбор лечебной тактики базируется на оценке общего состояния пациента, функциональных возможностей организма, ожидаемой эффективности и токсичности противоопухолевой терапии. Задачами противоопухолевой терапии являются – 1) улучшение качества жизни, 2) – увеличение продолжительности жизни.
Несмотря на значительные достижения современной науки в лечении рака желудка лекарственными противоопухолевыми препаратами, основным методом лечения рака желудка является хирургический.
Лучевая терапия, химиолучевая терапия
Данный вид лечения применяют в следующих ситуациях: наличие остаточной опухоли после хирургического вмешательства (обозначается как R2-резекция желудка), наличие опухолевых клеток в краях резекции, найденных при патоморфологическом (гистологическом) исследовании операционного материала (обозначается как R1-резекция желудка), а также при недостаточном объеме выполненной лимфодиссекции.
Химиолучевую терапию начинают на 29-й день после операции, на первом этапе проводят сначала цикл химиотерапии, затем начинают лучевую терапию в комбинации с химиотерапией.
Химиолучевая терапия может быть применена и для лечения изолированных местных рецидивов.
Динамическое наблюдение
Под динамическим наблюдением подразумевают регулярный сбор жалоб, данных осмотра пациентов, проведение лабораторных и инструментальных исследований пациентам, которым было проведено первичное радикальное лечение рака желудка, с целью раннего выявления местного рецидива и/или прогрессии заболевания в виде появления отдаленных метастазов. Осмотр и исследования проводятся в соответствии с определенным графиком – программой мониторинга. В соответствии с программой мониторинга лабораторные и инструментальные исследования проводятся сначала каждые 3 месяца, затем каждые 3-6 месяцев, далее – ежегодно.
Профилактика
Современная статистика отмечает рост смертности от злокачественных новообразований желудочно-кишечного тракта. Основная причина такой ситуации во многом связана с недостаточной информированностью общества о необходимости своевременной диагностики и профилактики заболеваний пищеварительных органов.
При наличии у человека тех или иных факторов риска, профилактикой развития рака желудка, будет являться устранение фактора(ов) риска.
- Борьба с хеликобактерной инфекцией. Для диагностики наличия хеликобактерной инфекции используются различные способы, самым простым из которых является уреазный дыхательный тест. Он абсолютно безболезненный и не требует никаких инвазивных вмешательств. После того, как выявлено наличие Helicobacter pylori по результатам дыхательного теста – проводят лечение данной инфекции. Эрадикация, то есть полное уничтожение, Helicobacter pylori может препятствовать развитию рака желудка, однако, если произошла злокачественная трансформация клеток слизистой оболочки желудка, данное лечение уже не эффективно. Именно поэтому своевременной и ранней диагностике предраковых состояний уделяется так много внимания. Ведь болезнь легче предупредить, чем лечить.
- При наличии воспалительных изменений стенки желудка - на фоне хронического гастрита, язвенной болезни желудка или дуодено-гастрального рефлюкса, профилактикой развития рака желудка будет являться непосредственное лечение данных заболеваний под контролем специалиста, как правило, врача-гастроэнтеролога.
- При наличии полипа или полипов желудка основной мерой профилактики будет удаление полипа (полипов) эндоскопическим путем во время гастроскопии.
- При наличии кишечной метаплазия желудка показаны регулярные профилактические осмотры врачом, выполнение гастроскопии, для исключения развития рака желудка. При регулярных профилактических осмотрах удается выявить рак желудка на ранней стадии и выполнить его успешное лечение.
- При наличии генетической предрасположенности показано прохождение программы скрининга рака желудка в более раннем возрасте. Рекомендуется выполнить диагностическую гастроскопию не позже срока соответствующему возрасту родственника, у которого был диагностирован рак желудка, минус 10 лет. Таким образом, если рак желудка был диагностирован у Вашего ближайшего родственника в возрасте 43 лет, то Вам необходимо впервые пройти диагностику (гастроскопию) в возрасте 33 лет. Периодичность профилактических осмотров и гастроскопии определяется врачом который Вас наблюдает.
- Рекомендуется отказаться от курения для снижения риска развития рака желудка.
- Рацион, включающий свежие овощи и фрукты, диетические сорта мяса и морепродукты, снижает риск возникновения злокачественных процессов в желудке. Предупреждает рак и употребление продуктов с высоким содержанием антиоксидантов. Наличие в питании продуктов с витаминами А, С и Е, а также селена снижает вероятность рака даже у людей со скудным рационом питания. Кроме того, по данным ВОЗ, ожирение входит в число факторов развития рака желудка. Рекомендуется поддерживать оптимальную массу тела, соблюдая равновесие между получаемыми с пищей калориями и их расходом. Данный баланс обеспечивает физическая активность и занятия спортом.
Для диагностики и лечения рака желудка вы можете обратиться в наше Хирургическое отделение N2 Университетской клинической больницы N4 в Москве. У нас работают специалисты высочайшего уровня, которые используют самое современное оборудование для постановки точных диагнозов и проведения эффективных операций.
- «Surgery for Gastric Cancer» Sung Hoon Noh, Woo Jin Hyung
- Отделение диагностической и лечебной эндоскопии, Университетская клиническая больница №2, Сеченовский Университет.


























